理論化学
化学講座 第21回:酸化と還元③「酸化剤と還元剤・酸化還元反応式」
最後に、酸化還元反応の反応式の作り方を説明します。さっき覚えた酸化剤と還元剤の半反応式を組み合わせて、酸化剤と還元剤の反応式を作る方法を説明します。この反応式にはイオン反応式と全反応式の2種類があります。
例として、硫酸酸性化マンガン酸カリウムとシュウ酸の反応式を考えます。
まず、両方の半反応式を書きます。
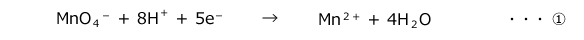
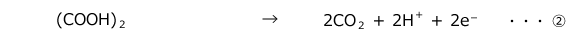
そして、次に、両辺のe-が等しくなるようにそれぞれの半反応式を整数倍して足し合わせ、両辺のe-を相殺します。
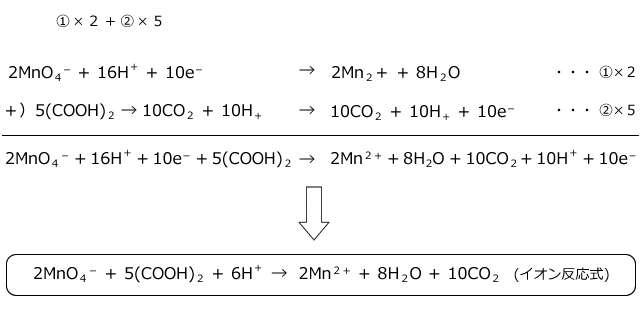
そうすると、両辺から電子が消えて、イオンを含んだ反応式が得られますね。このイオンを含んだ反応式をイオン反応式と呼びます。
さて、最後に、イオン反応式に登場しなかったイオンを加えて、イオンが出てこない反応式を作りますが、この反応式を全反応式と呼びます。
まず、左辺に着目します。MnO4-はK+を補ってKMnO4にします。そして、硫酸酸性ですから、H+はH2SO4にします。
そうすると、左辺にK+を2 つ、SO42-を3 つ加える事になりますね。当然、左辺だけに加えたのではいけません。右辺にも同じものを加えます。
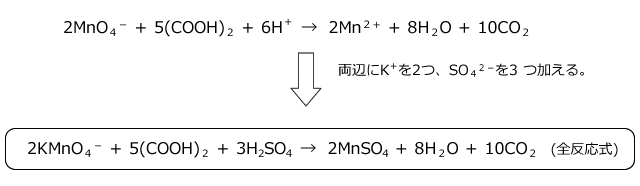
そうすると、イオンを含まない反応式ができます。この反応式を全反応式と言います。
はい、これで酸化還元反応の反応式を書くことができるようになりましたが、ここまでの手順をまとめておきましょう。
- 酸化剤・還元剤の半反応式を書く
- イオンの数を同じにして足し合わせる事により、電子を消した式を作る。(イオン反応式)
- 登場していないイオンを加えて、式からイオンを消す(全反応式)
今回はこれでおしまいです。お疲れ様でした。半反応式は今日中に覚えてくださいね。では、また、さようなら。