理論化学
無機化学
第2回 金属イオンの沈殿
今回は、無機化学で頻出の、金属イオンの沈殿の生成について解説します。
金属イオンの沈殿
沈殿する陽イオンと陰イオンの組み合わせと、生じる沈殿の色を覚える事が大切ですが、なかなか全て覚えるのは大変です。
そこで、便利なゴロを使いながら覚えてしまいましょう。これと錯イオンの生成を覚えてしまえば陽イオン分析は100発100中、必ず解答することができるようになります。
1. Cl- によって沈殿する陽イオンと沈殿の色
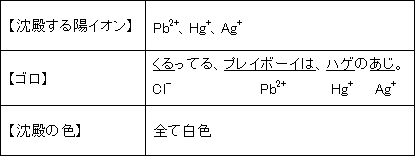
この中でちょっと注意しておかなくてはいけないのが、PbCl です。これは、冷水には溶けませんが、熱水には溶けます。それから、Hg+ です。HgCl ではなく、Hg2Cl2 の形で沈殿します。ちなみに、Hg は、Hg+ とHg2+ の二種類の陽イオンがありますが、HgCl2 の方は水によく溶けます。これもあわせて覚えておきましょう。
2. SO42-、CO32- によって沈殿する陽イオンと沈殿の色

SO42- で沈殿する Ba2+、Ca2+、Sr2+ はすべてアルカリ土類金属です。一方、同じ二族元素の 二族典型元素、Be2+、Mg2+ は SO42- によって沈殿しません。このように、アルカリ土類金属と 二族典型元素は性質が異なります。ほかにも、アルカリ土類金属は炎色反応をするのに対して二族典型元素は炎色反応を示さないなど、多くの性質の違いを持ちます。
CO32- は沈殿を作る能力が非常に高い陰イオンで、多くの陽イオンを沈殿させます。沈殿しにくいイオンはアルカリ金属くらいで、Be2+ や Mg2+ も CO32- とは沈殿を作ります。
CaCO3 の沈殿が生じた後、さらに CO2 を吹き込み続けると CaCO3 の沈殿は溶解して透明になりますが、この水溶液を加熱すると、過剰に吹き込んだ CO2 が追い出されて再び CaCO3 が沈殿します。
-
CaCO3 の溶解
CaCO3 + CO2 + H2O → Ca(HCO3)2
-
CaCO3 の再沈殿
Ca(HCO3)2 → CaCO3 + CO2 + H2O
3. CrO42- によって沈殿する陽イオンと沈殿の色

ここから、沈殿に色が付き始めます。ゴロの中に色も入っているので、あわせて覚えましょう。
ところで、CrO42-(クロム酸イオン)は沈殿を作る能力の高い陰イオンですが、同じ六価のクロムを含む Cr2O72-(ニクロム酸イオン)は沈殿を作る能力が低く、Ag+、Pb2+、Ba2+ と反応させ て生じる沈殿は、結局、AgCrO4、PbCrO4、BaCrO4 です。
4. H2S(すべての液性)によって沈殿する陽イオンと沈殿の色

S2- は様々な金属と沈殿を作ります。また、液性によって生じる沈殿が違うので泉意が必要ですが、なぜ、液性によって変わるのかというと、H2S の電離度が液性によって異なるからです。
H2S は酸性の化合物なので、酸性の水溶液中では電離度が小さく、S2- の濃度は非常に小さくな ります。そのために溶解度積の比較的大きな金属は、酸性水溶液中では沈殿を生じないのです。
一方、ここに出てきている金属は、溶解度積が比較的小さいため、S2- の濃度の小さな酸性水溶液中でも沈殿を生じるのです。
また、ここで沈殿する水銀イオンは、Hg+ ではなく、Hg2+ であることにも注意しておいてください。
※ははにいおう → H、H に硫黄 → H2S というこじつけです。
5. H2S(中性、塩基性)によって沈殿する陽イオンと沈殿の色

Whyはわかりにくいと思いますが、Why → White → 白 と連想してください。
当然、中性、塩基性の時も 4. のイオンたちは沈殿します。
6. OH- によって沈殿する陽イオン

OH- は沈殿を作る力が非常に強く、アルカリ金属、アルカリ土類金属以外の金属はすべて沈殿します。上にあげた陽イオンは入試でよく問われる、重要なものだけです。逆に、これだけ覚えておけば入試ではまず安心です。
Hg2+ と Ag2+ は水酸化物ではなく、酸化物が沈殿します。Ag+ は狙われやすいので注意してください。また、そのほかの水酸化物は沈殿を加熱乾燥すると酸化物になります。(これは別の回で解説します)
ここはすっきりしたゴロがなく、ちょっと大変かもしれませんが、頑張って覚えてください。