理論化学
化学講座 第18回:酸と塩基(5)
NaOHとNa2CO3はともに塩基として働きます。この2種類の塩基の混合物に含まれているNaOHとNa2CO3のそれぞれの物質量を測定したいとしたらどうしたらいいでしょうか。
その方法が、二段滴定(ワルダー法)なのです。
2)二段滴定(ワルダー法)
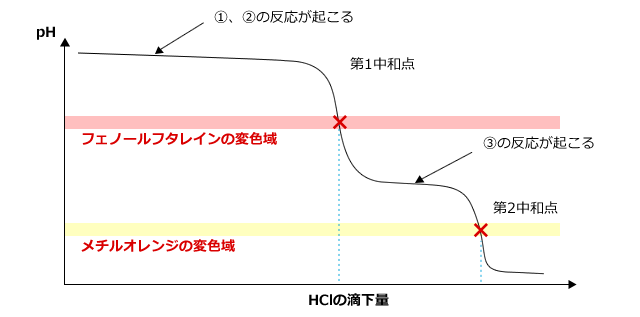
NaOHとNa2CO3の混合物を水に溶かした水溶液(混合水溶液)をHClで滴定していくと、下図のように、中和点を二つ持つ滴定曲線が得られます。
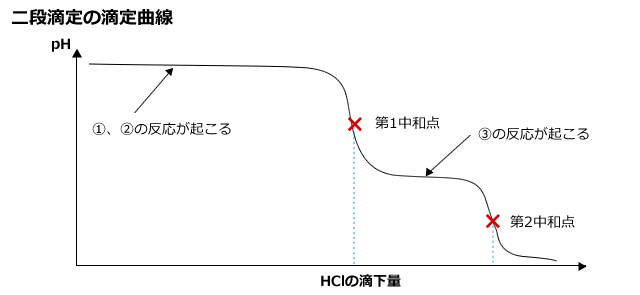
なぜこのような滴定曲線が得られるのでしょうか。
NaOHとNa2CO3の混合水溶液にHClを滴下していくと、次の①、②、③の反応が起こりますね。
NaOHとHClの反応
NaOH + HCl → NaCl + H2O ・・・・ ①
Na2CO3はHClと次のように2段階でHClと反応します。
Na2CO3 + HCl → NaHCO3 + NaCl ・・・・ ②
NaHCO3 + HCl → H2O + CO2 + NaCl ・・・・ ③
で、実は、中和反応には、強い塩基から反応し、より強い塩基が反応している間は、弱い塩基は反応できないというルールがあるのです。
塩基としての強さは、NaOH > Na2CO3 > NaHCO3の順ですから、NaOHとNa2CO3の混合物にHClを加えていくと①→②→③の順に反応が起こります。
最初に①の反応が起こってNaOHだけがHClと反応し、NaOHが全て反応し終わると②の反応でNa2CO3 がHClと反応し、全て NaHCO3 になってから③の反応でNaHCO3がHClと反応するのです。
ここで、NaOH は強い塩基性、Na2CO3 はやや強い塩基性を示し、共にフェノールフタレインを赤色に変色させます。一方、 NaHCO3は弱い塩基性で、フェノールフタレインを変色させませんが、メチルオレンジは黄色に変色させます。
ですから、NaOH と Na2CO3 の混合水溶液にフェノールフタレインを加えてHClを滴下すると、①と②の反応が終了して、NaOH と Na2CO3 のみになったときに溶液の色が透明になります。これが第一中和点です。
さらに、メチルオレンジを滴下して滴定を続けると、③の反応が起こって NaHCO3がHCl とはんのうします。そして、NaHCO3がすべて反応してしまうと溶液が赤色に変化します。これが第二中和点です。
そうそう、③の反応で、右辺にH2CO3と書くと誤りです。H2CO3は弱酸ですから強酸のHClによって追い出されてH2OとCO2になってしまいます。模試などでも多い間違いですから、気を付けてくださいね。