理論化学
化学講座 第29回:電気分解【ファラデーの法則】
例題6)
- 銅板を陰極、炭素を陽極にして塩化銅(Ⅱ)水溶液を電気分解すると、陰極に銅が2.54 g析出した。塩素は水に溶けないものとする。陽極で発生した塩素は0℃、1.01×105 Pa(1atm)で何mLか。
(解答)
こちらも、陽極と陰極での反応を書きます。
陽極での反応: 2Cl- → Cl2 + 2e- ・・・・ ① 陰極での反応: Cu2+ + 2e- → Cu ・・・・ ② 陰極に生じた銅は
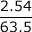 = 0.040 mol である。回路に流れた電子の物質量を χ molとすると
= 0.040 mol である。回路に流れた電子の物質量を χ molとすると
陽極に生じた Cl2 の体積を y L とします。通過した電子の物質量は陰極と同じですから

もちろん、例題5)のように、①と②から電子を消して全体の反応式を出して、析出した銅の物質量と、発生する塩素の体積V Lを求めるという方法もあります。
今回はファラデー定数を用いて電子の物質量と電気量を変換することを説明しました。次回は直列接続の電気分解と並列接続の電気分解など、私大医学部入試でもよく取り上げられる、実戦的な問題について説明します。