第18回:酸と塩基(5)
例題
n1molのNaOHとn2molのNa2CO3の混合物を水に溶かしてフェノールフタレインを数滴加えた。
a mol/ℓのHClを滴下すると、滴下量がv0mℓの時にフェノールフタレインの赤色が消えた。
次にメチルオレンジを加えて更にHClを滴下すると、総滴下量がv1 mℓの時に水溶液の色が赤色になった。このとき、n1とn2を求めなさい。
(解答・解説)
第1中和点は、①と②の反応が終わったところですね。ここまでの滴下量がv0 mℓ。
第2中和点までの総滴下量はv1mℓですから、②の反応で生じたNaHCO3の中和にはv1-v0 mℓのHCl水溶液が必要ということになります。
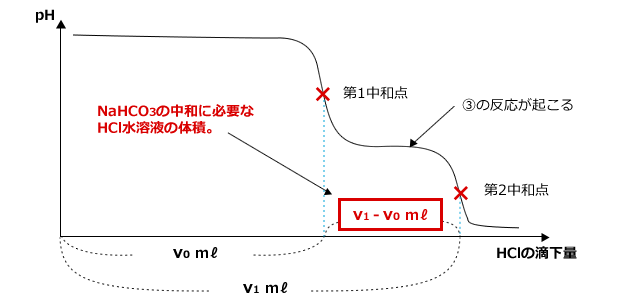
ここで、最初のNa2CO3とHClが反応して生じたものですから、③で反応したNaHCO3の物質量ともともと存在していたNa2CO3の物質量は同じです。
ということは、②の反応で必要なHCl 水溶液の体積は、③の反応で必要なHCl 水溶液の体積と同じ
v1-v0 mℓということになりますね。
従って、Na2CO3と反応したHClの体積は
2(v1-v0)mℓであり、①で反応したHClはv0-(v1-v0)mℓ=2v0-v1mℓとなります。
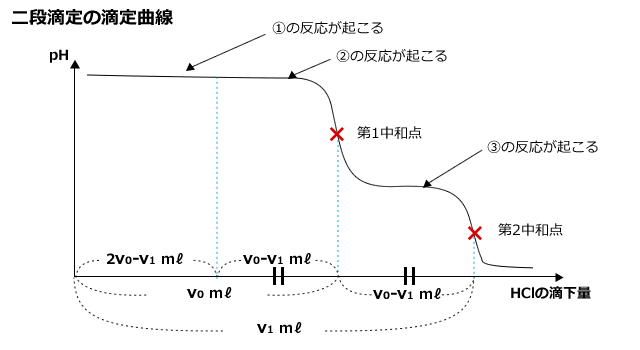
ここまでくれば、あとは【H+の物質量】=【OH-の物質量】式を作ってn1とn2を求めるだけです。
NaOHについて:a×![]() ×1=n1×1 よりn1=a×
×1=n1×1 よりn1=a×![]() mol
mol
Na2CO3について:a×2(v1-v0)×1=n2×2 より n2=a×(v1-v0) mol
今日は、二段滴定と逆滴定の説明を行いました。難易度が高いとされる問題ですが、やってみると意外と簡単でしたね。
NaOHとNa2CO3の混合物の純度を求める方法には、二段滴定(ワルダー法)以外に、ウインクラー法というものもあります。これも頻出問題ですから、図説などを使って調べておいた方がいいでしょうね。

平野 晃康
株式会社CMP代表取締役
私立大学医学部に入ろう.COM管理人
大学受験アナリスト・予備校講師
昭和53年生まれ、予備校講師歴13年、大学院生の頃から予備校講師として化学・数学を主体に教鞭を取る。名古屋セミナーグループ医進サクセス室長を経て、株式会社CMPを設立、医学部受験情報を配信するメディアサイト私立大学医学部に入ろう.COMを立ち上げる傍ら、朝日新聞社・大学通信・ルックデータ出版などのコラム寄稿・取材などを行う。

