化学連載 第53回:化学反応速度④反応における熱の出入り
前回は反応のメカニズムと反応速度の式について説明しました。
今回は、反応に伴って出入りする熱量について説明します。
反応に伴う熱量を説明するには、下図のように横軸に反応の進行、縦軸に物質の持つポテンシャルエネルギーを取った図を利用します。前回使ったモデル A+B → C を使って説明します。
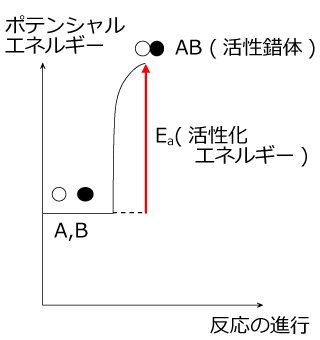
左図のように、反応物 A、B が活性錯体 AB になるには持っているエネルギーの差分を吸収しなくてはいけません。このエネルギーの差分を活性化エネルギー Ea といい、このエネルギーは反応物 A、B の持っていた運動エネルギーから吸収されます。A、B の持っている運動エネルギーが活性化エネルギーに満たない場合は活性錯体は生じず、A と B は反発して再びバラバラに動きます。
活性錯体 AB が生成物 C になるとき、発熱が起こりますが、この発熱 量 Q1 が Ea より大きいときはその差分の Q1 - Ea が外部に放出される発熱反応、逆に Ea より小さいときはその差分 Ea - Q1 が外部から吸収される吸熱反応となります。
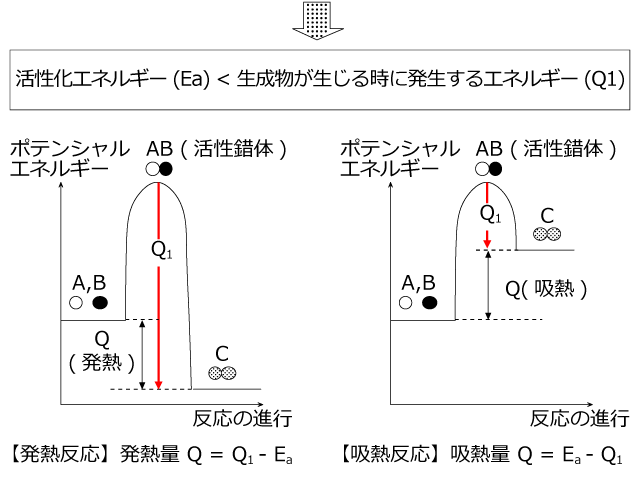
反応前後での熱の出入りの量は、生成物と反応物の持っているポテンシャルエネルギーの差だということが分かりますね。従って、逆反応では正反応と同じ大きさで吸熱と発熱が逆になった熱量が出入りします。
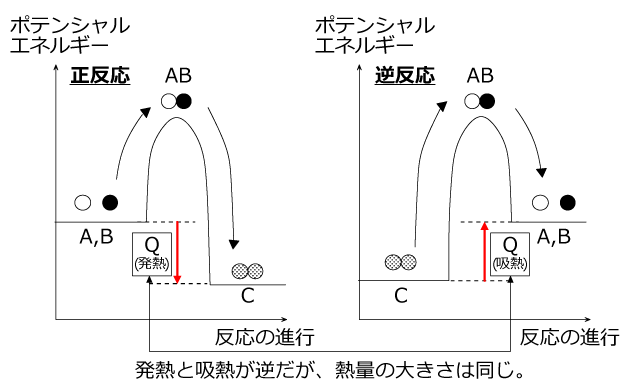
次は、触媒を使った場合の熱量について考えてみます。触媒というのは、そのものは反応の前後で変化しないが、反応速度を大きくする性質のある物質です。これは、触媒を用いると活性化エネルギーが減少するためです。どうして活性化エネルギーが小さくなるのかというと、活性錯体がエネルギー的に安定なためです。
触媒にはいくつか種類がありますが、その一種の吸着触媒を使ってH2 + I2 → 2HIの反応を例に説明します。

気相でこの反応を進めると、活性錯体は H2I2 という形になります。これは非常に不安定ですので、I2 と H2 という状態からこれを生成するには、大きな活性化エネルギーが必要になります。
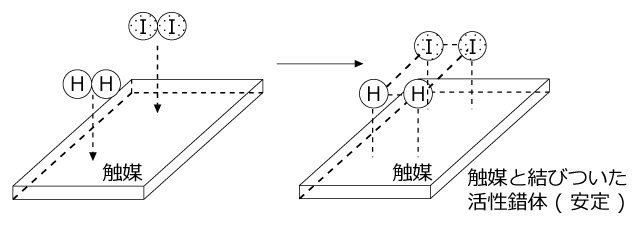
一方、触媒が存在する場合は、H2 と I2 がいったん触媒と結びつきます。すると、H2 、I2 の内部の共有結合がゆるくなって上図右側のような状態になります。これが、触媒と結びついた状態の活性錯体で、触媒と結びついている分だけ安定です。したがって、触媒がある場合は活性化エネルギーが小さくて済むのです。
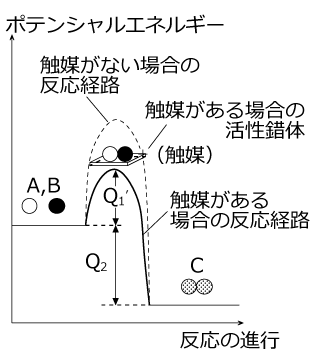
エネルギーと反応の進行のグラフは右図のようになります。
活性化エネルギーが少なくて済む分、反応物が衝突した際に活性錯体になる場合の割合が大きくなり、そのため、反応速度は速くなります。しかし、反応の最初と最後のエネルギー状態 ( 反応物や生成物が持っているエネルギー ) が変化するわけではないので、反応熱の大きさは変化しません。

平野 晃康
株式会社CMP代表取締役
私立大学医学部に入ろう.COM管理人
大学受験アナリスト・予備校講師
昭和53年生まれ、予備校講師歴13年、大学院生の頃から予備校講師として化学・数学を主体に教鞭を取る。名古屋セミナーグループ医進サクセス室長を経て、株式会社CMPを設立、医学部受験情報を配信するメディアサイト私立大学医学部に入ろう.COMを立ち上げる傍ら、朝日新聞社・大学通信・ルックデータ出版などのコラム寄稿・取材などを行う。

